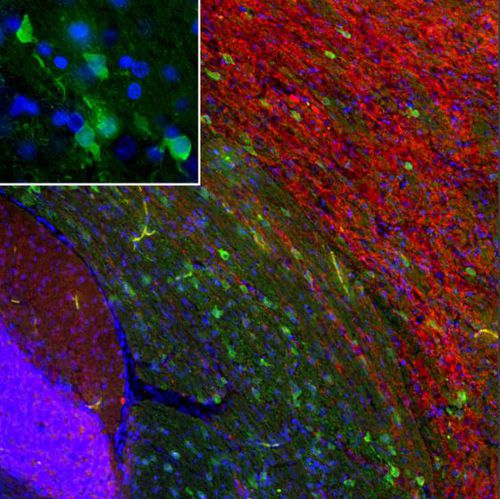
Реактив IgG MO22196для вестерн-блоттингадля иммунофлюоресценциидля иммуноцитохимии
Добавить в папку «Избранное»
Добавить к сравнению
Характеристики
- Тип
- IgG
- Применение
- для вестерн-блоттинга, для иммунофлюоресценции, для иммуноцитохимии
- Формат
- жидкость
- Тестируемый маркер
- PEA15
- Происхождение
- на основе мыши
- Температура хранения
МАКС.: 4 °C
(39 °F)МИН.: -20 °C
(-4 °F)
Описание
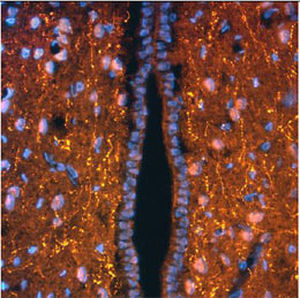
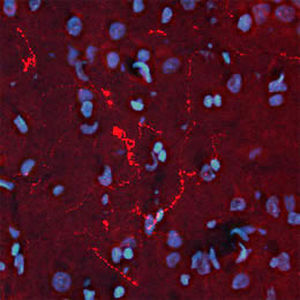
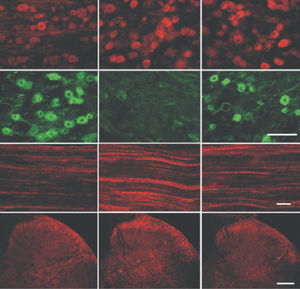
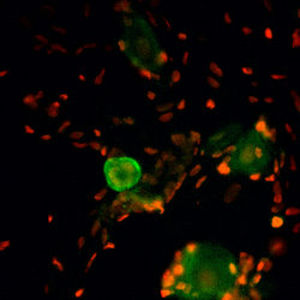
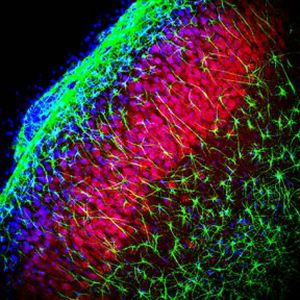
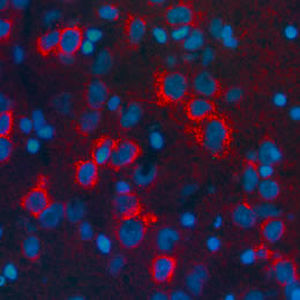
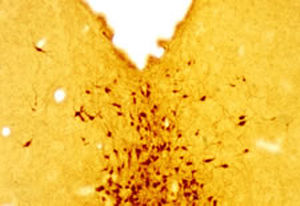
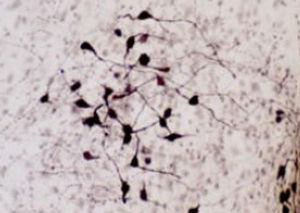
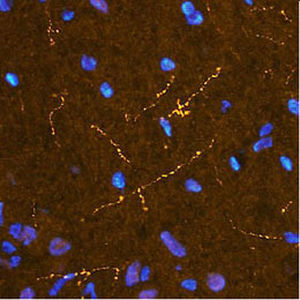
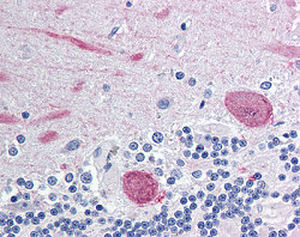
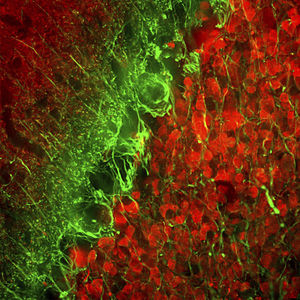
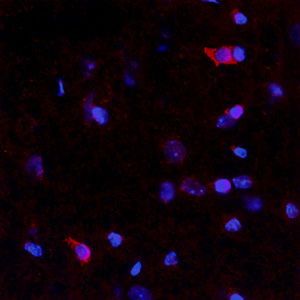
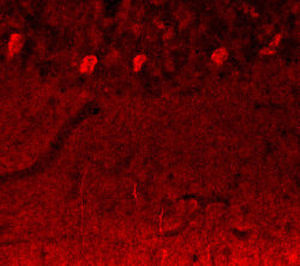
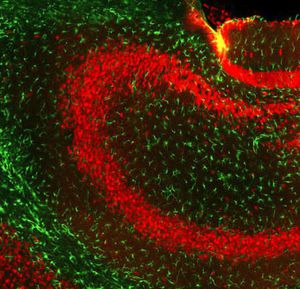
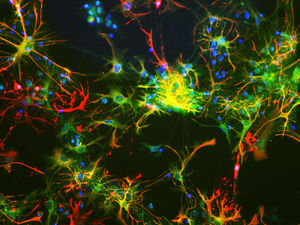
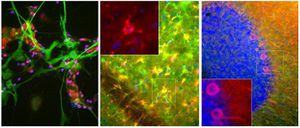
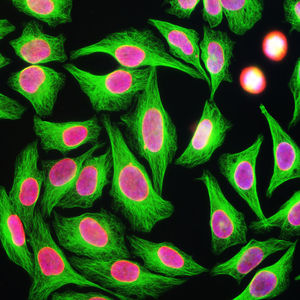
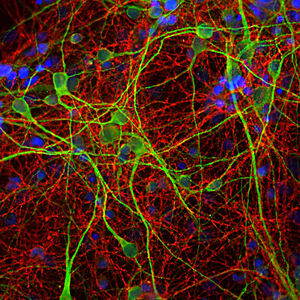
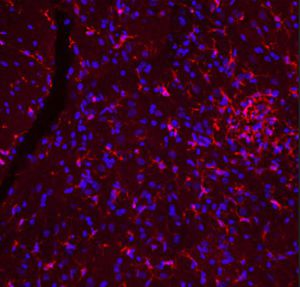
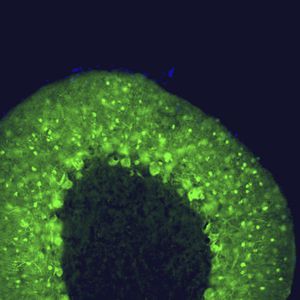
Первоначально PEA-15 был выделен как основной низкомолекулярный белок из эмбриональных стриатных астроцитов мыши, выращенных в культуре клеток. Три пятна на двумерных гелях с кажущейся молекулярной массой 15 кДа и изоэлектрической точкой 5,1-5,3 были показаны как различные формы одного белка. Белок фосфорилировался серином на одном участке протеинкиназой С как in vivo, так и in vitro, и белок был назван "фосфопротеином, обогащенным в астроцитах 15 кДа", отсюда PEA-15. Последующее клонирование и секвенирование выявило белок, хорошо сохранившийся по последовательности между мышью и человеком и интенсивно экспрессирующийся в мозге. Независимо от этого тот же белок был обнаружен в фибробластах и тканях больных диабетом и назван "белком, обогащенным при диабете" или PED. Иммуноцитохимические исследования показали, что белок интенсивно экспрессируется в астроцитах и некоторых нейронах в ЦНС мышей, хотя повсеместно он экспрессируется на более низком уровне. Было показано, что PEA-15 взаимодействует с киназой, регулирующей внеклеточный сигнал, и регулирует ядерный вход этого белка, а также описано несколько других важных взаимодействий с другими белками, участвующими в регуляции апоптоза, метаболизма глюкозы и клеточного роста. MCA-4D2 был создан против рекомбинантной полноразмерной конструкции PEA-15, экспрессированной и очищенной из E. coli.
---
Каталоги
Для этого товара не доступен ни один каталог.
Посмотреть все каталоги NeuromicsДругие изделия Neuromics
Primary Antibodies
Расширенный поиск
- Набор реактивов
- Реактив для молекулярной биологии
- Набор реактивов жидкость
- Набор реактивов для исследований
- Набор реактивов для протеинов
- Набор реактивов для иммуноанализа
- Набор реактивов антитела
- Лиофилизированный набор реактивов
- Набор реактивов сыворотки
- Набор реактивов для иммуногистохимии
- Набор реактивов моноклональное антитело
- Набор реактивов для научных исследований
- Набор реактивов для вестерн-блоттинга
- Набор реактивов для иммунофлюоресценции
- Набор реактивов поликлональное антитело
- Набор реактивов цитокин
- Набор реактивов фактор роста
- Реактив на основе мыши
- Реактив IgG
- Реактив для иммуноцитохимии
* Цены указаны без учета налогов, без стоимости доставки, без учета таможенных пошлин и не включают в себя дополнительные расходы, связанные с установкой или вводом в эксплуатацию. Цены являются ориентировочными и могут меняться в зависимости от страны, цен на сырьевые товары и валютных курсов.